电池电化学:跨越时空的能量舞蹈
TL;DR
- 能量转换器:电池是将化学能(吉布斯自由能 $/Delta G$)与电能相互转换的装置。放电是自发过程,充电是非自发过程。
- 多孔电极(Porous Electrode):商业电池的电极不是平板,而是由活性物质、导电剂、粘结剂组成的多孔结构,充满电解液,以最大化反应面积。
- 多尺度动力学:电池内部发生着跨越多个时间尺度的过程——从微秒级的欧姆极化,到秒级的电荷转移,再到分钟/小时级的固相扩散。
- 建模与表征:为了理解这个复杂的黑盒子,我们需要将**电化学建模(Modeling)与实验表征(Characterization)**相结合,互为验证。
1. 电池的基本解剖学
一个典型的电化学池(Electrochemical Cell)包含三个核心部分:
- 阳极(Anode):发生氧化反应(失去电子)的电极。在放电时是负极,充电时是正极(但习惯上我们常称负极为Anode)。
- 阴极(Cathode):发生还原反应(得到电子)的电极。
- 电解质(Electrolyte):离子导体,电子绝缘体。它像一座桥,只允许离子通过,迫使电子走外电路做功。
商业电池的微观结构
在实验室里,我们可能用平板电极。但在商业电池中,为了获得高功率,电极被设计成多孔结构(Porous Structure)(如图1):
- 活性物质(Active Material):真正干活的(如LFP, 石墨),负责储存锂离子。
- 导电剂(Conducting Agent):如炭黑(Super P),构建电子的高速公路。
- 粘结剂(Binder):如PVDF, SBR,把大家粘在一起,防止掉粉。
- 孔隙(Pore Space):充满电解液,构建离子的传输通道。
这种设计大大增加了反应表面积,但也带来了复杂的传输路径(曲折度)。
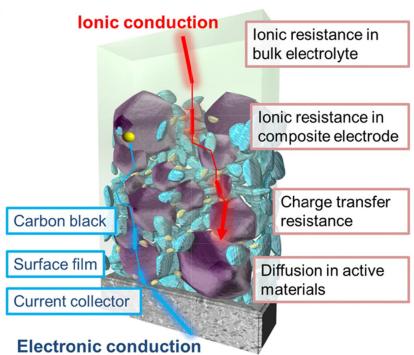 图1. 多孔电极内部的电子与离子传输路径。
图1. 多孔电极内部的电子与离子传输路径。
2. 热力学:驱动力的来源
电池为什么能放电?因为反应物(高能态)想变成产物(低能态)。这种化学驱动力由**吉布斯自由能变化($/Delta G_r$)**描述:
$$ /Delta G_r^/circ = -nFE^/circ $$
- $n$:电子转移数。
- $F$:法拉第常数。
- $E^/circ$:标准电动势(OCV)。
这个公式告诉我们:化学能的降低($/Delta G < 0$)直接转化为了电能($E > 0$)。
3. 动力学:时间的魔法
虽然热力学决定了电池“能不能”放电,但动力学决定了它“能放多快”。电池内部的反应像一场接力赛,速度由最慢的一棒决定(决速步)。
时间尺度的跨越
当我们给电池通电时,不同物理过程的响应速度是完全不同的:
- 微秒级($/mu s$):欧姆极化(Ohmic)。电子在集流体和颗粒间的传导,瞬间发生。
- 毫秒级($ms$):双电层充电。离子在界面处的重新排列。
- 秒级($s$):电荷转移(Charge Transfer)。锂离子跨越固液界面(SEI膜)脱溶剂化并嵌入。
- 分钟/小时级:固相扩散(Solid-state Diffusion)。锂离子在活性颗粒内部的缓慢爬行。
- 小时级:浓差极化。电解液中离子浓度的宏观梯度建立。
这就是为什么我们在做**EIS(阻抗谱)**时,能通过频率把它们一个个区分开来。
4. 为什么需要建模?
电池内部是一个“黑箱”,充满了多物理场耦合(电、热、化学、力学)。
- 跨尺度挑战:从埃米级的晶格跳跃,到微米级的颗粒扩散,再到毫米级的极片传输,最后到米级的电池包管理。
- 实验的局限:实验只能测到外部的电压、电流、温度,很难直接看到内部的锂浓度分布或局部电位。
这时候,**电化学模型(如P2D模型)**就成了我们的“虚拟显微镜”,它能帮我们推断内部发生了什么,验证实验猜想,并指导下一代电池的设计。
[精工博研] 负极材料的"工业级"验证专家
别让扣电数据掩盖材料的真实性能。
我们提供从粉末到圆柱全电池的一站式验证服务,用头部电池厂的标准(Enterprise Standards)为您提供"通行证"级别的数据报告。
- 全电池试制:圆柱电池全流程加工(涂布/卷绕/化成),还原真实极片应力。
- 极限快充:6C/10C 循环测试,验证材料在超充时代的真实寿命。
- 微观工艺:OI值(取向度)与极限压实分析,解决极片加工痛点。
- 全气候验证:-20℃~60℃ 放电及 55℃ 高温储存,确保极端环境可靠性。
欢迎联系我们 19939716636
 图1. 多孔电极内部的电子与离子传输路径。
图1. 多孔电极内部的电子与离子传输路径。

 首页
首页
 检测领域
检测领域
 服务项目
服务项目
 咨询报价
咨询报价